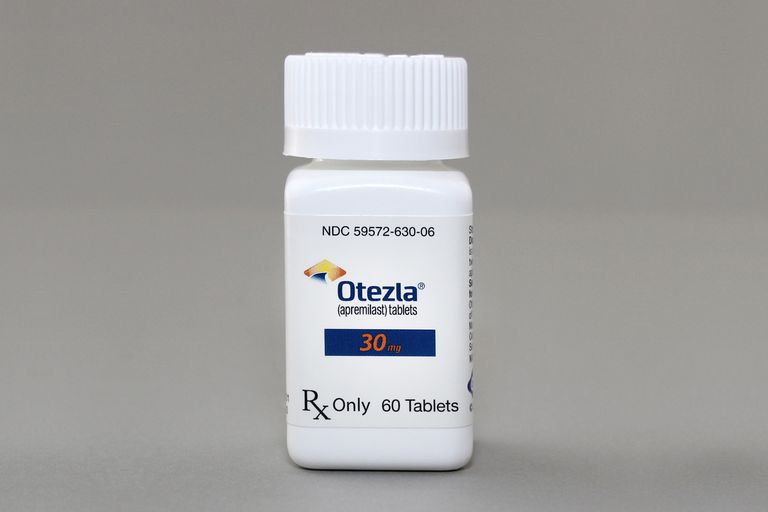
Am 21. März 2014 gab die FDA die Zulassung von Otezla (Apremilast) zur Behandlung von aktiver Psoriasis-Arthritis bei Erwachsenen bekannt. Otezla ist ein selektiver Inhibitor von Phosphodiesterase-4 (PDE4). Otezla ist die einzige von der FDA zugelassene orale Behandlung speziell gegen Psoriasis-Arthritis. Am 23. September 2014 genehmigte die FDA Otezla für eine zusätzliche Indikation, die Behandlung von Patienten mit mittelschwerer bis schwerer Plaque-Psoriasis, für die eine Phototherapie oder systemische Therapie geeignet ist.
Vor der Zulassung von Otezla wurde Psoriasis-Arthritis typischerweise mit Kortikosteroiden, TNF-Blockern oder Stelara (Ustekinumab), einem Interleukin-12 / Interleukin-23-Inhibitor, der im September 2013 zugelassen wurde, behandelt.
Wie wird Otezla verabreicht?
Otezla kommt als rautenförmige Filmtabletten in drei Stärken: 10 mg, 20 mg und 30 mg. Die anfängliche empfohlene Dosierung von Otezla beinhaltet eine Titration vom ersten bis zum fünften Tag, um die empfohlene Erhaltungsdosis von 30 mg zu erreichen. zweimal täglich ab Tag 6. Der übliche Titrationsplan ist:
Tag 1: 10 mg. am Morgen
Tag 2: 10 mg. am Morgen und 10 mg. abends
3. Tag: 10 mg. am Morgen und 20 mg. abends
Tag 4: 20 mg. am Morgen und 20 mg. abends
Tag 5: 20 mg. am Morgen und 30 mg. abends
6. Tag und danach: 30 mg. am Morgen und 30 mg. abends
(Hinweis: Patienten mit schwerer Nierenfunktionsstörung müssen Anpassungen am Dosierungsschema vornehmen). Welche gemeinsamen Nebenwirkungen wurden mit Otezla in Verbindung gebracht?
In klinischen Studien waren Durchfall, Kopfschmerzen und Übelkeit die am häufigsten berichteten Nebenwirkungen, die mit Otezla assoziiert sind. Die meisten unerwünschten Ereignisse traten innerhalb der ersten zwei Wochen der Behandlung auf und lösten sich im Laufe der Zeit mit fortgesetzter Anwendung von Otezla auf. Gibt es Kontraindikationen oder Warnungen und Vorsichtsmaßnahmen im Zusammenhang mit Otezla?
Otezla ist bei Patienten mit bekannter Überempfindlichkeit gegen Apremilast kontraindiziert. In Bezug auf Warnhinweise und Vorsichtsmaßnahmen ist Otezla mit einem erhöhten Risiko für Depressionen verbunden. Eine Gewichtsabnahme wurde auch in klinischen Studien als mögliches unerwünschtes Ereignis festgestellt. Patienten sollten auf unerklärliche und klinisch signifikante Gewichtsabnahme achten.
Es kann auch eine mögliche Arzneimittelwechselwirkung zwischen Otezla und Cytochrom P450-Enzyminduktoren wie Rifampicin, Phenobarbital, Carbamazepin und Phenytoin geben, die die Wirksamkeit von Otezla verringern würden. Die Kombination wird nicht empfohlen.
Gut kontrollierte Studien mit Otezla wurden bei Schwangeren nicht durchgeführt. Otezla sollte während der Schwangerschaft nur dann angewendet werden, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus überwiegt. Es ist auch nicht bekannt, ob Otezla oder Metaboliten von Otezla in der Muttermilch vorhanden sind, deshalb muss die stillende Frau vorsichtig sein. Im Rahmen der FDA-Zulassung wird es ein Verzeichnis für Frauen geben, die schwanger sind und mit Otezla behandelt werden.
Wie hat Otezla in klinischen Studien durchgeführt?
Die Sicherheit und Wirksamkeit von Otezla wurde in drei klinischen Studien mit 1.493 Patienten mit aktiver Psoriasis-Arthritis untersucht.
In den Studien PALACE-1, PALACE-2 und PALACE-3 erhielten die Studienteilnehmer randomisiert Placebo, Otezla 20 mg. oder 30 mg. zweimal täglich. Die Patienten durften während der Studie mit DMARDs, niedrig dosierten Kortikosteroiden oder NSAIDs fortfahren. Der primäre Endpunkt war ACR20 bis Woche 16. Otezla plus DMARDs im Vergleich zu Placebo plus DMARDs war mit einer stärkeren Verbesserung der Anzeichen und Symptome der Psoriasis-Arthritis assoziiert. Es gab auch Hinweise auf eine stärkere Verbesserung der körperlichen Funktion mit Otezla (30 mg, zweimal täglich) als Placebo.
Was kostet Otezla?
Der Medikamentenhersteller Celgene hat für Otezla einen Großhandelspreis von 22.500 Dollar pro Jahr festgelegt.